Radioaktivitet og planter
Radioaktiviteten ble oppdaget i 1896 av den franske fysikeren Henri Becquerel. Radioaktivitet er en egenskap ved ustabile kjerner som desintegrerer til en mer stabil tilstand. Hastigheten som en radioaktiv isotop desintegrerer (forvandling i kjernen) med uttrykkes av den fysiskehalveringstiden. At atom (nuklide) kan beskrives som:

Hvert atom for et grunnstoff (element) (X) er karakterisert av kjernens sammensetning av protoner (Z) og nøytroner (N). Summen av antall protoner og nøytroner er like massetallet (nukleontallet (A). Ifølge Niels Bohr og Ernest Rutherfords atomteori består et atom av en kjerne omgitt av elektronskall. Antall elektroner rundt kjernen er lik antall protoner. Atomer kan avgi eller motta et ekstra elektroner og danne ioner, henholdsvis kationer eller anioner. Atomer med samme antall protoner, men med forskjellig massetall kalles isotoper av samme grunnstoff (gr. isotopos - samme plass). I elementenes periodiske system er grunnstoffenes ordnet etter atomnummer dvs. antall protoner i kjernen. Elementene i en gruppe (kolonne) har samme antall og type av ytre elektroner. De får derved også mange like kjemiske egenskaper. Hver periode (horisontalrad) nedover i det periodiske system betyr et nytt elektronskall. F.eks. hører cesium med til alkaliemetallene i gruppe 1 og har atomnummer 55. Cesium ble oppdaget i 1860 av R. Bunsen og G.R. Kirckhoff ved hjelp av spektralanalyse, og fikk navn etter en type blå spektrallinjen som cesium har (l. caesisus - himmelblå). Andre alkaliemetaller er natrium (Na), kalium (K) og rubidium (Ru). Innholdet av cesium er lavt i jordskorpen og cesium forekommer under naturlige betingelser bare som cesium-133 (133 Cs) med 55 protoner, og 78 nøytroner som gir massetallet 133. For enkelhets skyld angir man bare massetallet og navnet på nukliden.133 Cs er stabil og ikke radioaktiv. Det finnes imidlertid mange radioaktive isotoper av cesium bl.a. 134 Cs og137 Cs . Vi skal seinere se at plantene kan ta opp cesium fra jorda, og hva det betyr.

Naturlig forekommende radioaktive nuklider
Omtrent en tredjedel av grunnstoffene i det periodiske system har naturlig forekommende radioaktive isotoper. Disse radioaktive isotopene kan naturlig dannes på forskjellig måte:
A) Kosmisk stråling fra verdensrommet inneholder neutroner som kan fanges opp av grunnstoffer i atmosfæren f.eks. nitrogen og argon, og det er muligheter til å få dannet radioaktive isotoper som karbon-14 (14C), tritium (3H), svovel-35 (35S), natrium-22 (22Na), silisium-32 (32Si), fosfor-32 (32P) og fosfor-33 (33P). Tritium kan også komme fra sola og nå jordoverflaten.
B) Naturlig forekommende radioaktive nuklider med meget lang halveringstid er f.eks. kalium 40 (40K), rubidium-87 (87Rb), og de naturlige radioaktive serier
- 1) Uran-radiumserien som starter med 238U og ender med 206Pb
- 2) Thoriumserien 232Th 208Pb Þ
- 3) Actiniumserien 235U 207Pb. Þ
Ved desintegrasjonen av de radioaktive nuklidene kan det sendes ut stråling avhengig av type isotop i form av alfastråling, betastråling eller gammastråling. Dette gir en lav kontinuerlig naturlig bakgrunnsstråling.
Radioaktive nuklider produsert ved menneskelig aktivitet
Enrico Fermi oppdaget i 1935 at stabile grunnstoffer kunne bli radioaktive ved å bombardere dem med nøytroner. Nøytronene ble fanget inn og det ble dannet utstabile kjerner. Under kodenavnet "Manhatten prosjektet" ble det i USA under 2. verdenskrig utviklet atombomber basert på fisjonering av isotoper av uran eller plutonium. Når nøytroner treffer kjernen til 235U eller 239Pu deles kjernen i to deler og det frigis varme (termisk energi), gammastråler og nye nøytroner. Hvis man har nok spaltbar masse vil nye nøytroner kunne gi en kjedereaksjon hvor alt spaltbart materiale fisjonerer og gir en voldsom eksplosjon. Dette kan gjøres ved at to subkritiske masser bringes i kontakt med hverandre, eller ved at en subkritisk masse konsentreres i en implosjon. Fysikere som deltok i prosjektet var bl.a. Fermi, Einstein, Szilard, Bethe, Compton og Oppenheimer. Ildkulen, ildstormene, sjokkbølgene, direkte nøytroner og gammastråling dreper og utsletter alt i nærmeste kilometeromkrets. I tillegg kommer radioaktivt nedfall fra partikler og flyktige isotoper. Den 6. august 1945 ble en uranbombe sprengt over Hiroshima, og 9. august en plutoniumbombe over Nagasaki som endte med at Japan kapitulerte dagen etter. I de følgende år skaffet flere stormakter seg atomvåpen: Sovjetunionen 1949, Storbritannia 1952, Frankrike 1960, Kina 1964, India 1974 og Pakistan 1998. Dessuten regner man med at bl.a. Israel har atombomber. Edward Teller var en av dem som var med å utvikle en hydrogenbombe. Den høye temperaturen som en vanlig fisjonsatombombe skapte var nok til å kunne bruke den som en tennmekanisme for en fusjonsbombe hvor hydrogen (isotopene deuterium og tritium) blir omdannet til helium. Mens sprengkraften på fisjonsbomber måles i kilotonn (tilsvarende 1000 tonn TNT) blir hydrogenbombene angitt i megatonn (tilsvarende 1.000.000 tonn TNT). Den største bomben som ble sprengt hadde 50 megatonn. Det ble også laget nøytronbomber som har til formål å drepe mennesker, uten å ødelegge bygninger og infrastruktur. Nedfallet fra atombombeprøvene i atmosfæren på begynnelsen av 1960-tallet ga en betydelig økning av radioaktive isotoper over hele jordkloden. Det ble bygget atomkraftverk. Radioaktive isotoper som 14C, 32P, 35S brukt i metabolismestudier ga grunnlaget for en enorm utvikling av biokjemi, molekylærbiologi. Kobolt-60 (60Co) kunne brukes til bestråling av kreftsvulster. Jod-131 (131I) blir akkumulert i skjoldbruskkjertelen, og som en bieffekt kunne dette brukes til å studere sykdommer i denne kjertelen.
Skadevirkningene av radioaktive stoffer ble oppdaget før radioaktiviteten. Gruvearbeidere i Schneeberg og Joachimsthahl fikk lungekreft. I 1885 ble det brukt de lysende egenskapene til thorium-cerium oksid (Welshbach-gasmantel). Uranoksid ble brukt til å gi oransje farge på glass. Små mengder radium sammen med Zn-sulfid ga scintillasjon og ble brukt i lysende klokker, kompass og i lysende maling. For å få tynne streker slikket de kvinnelige arbeiderne på penselen og resultatet ble beinkreft. Leukemi var en relativt sjelden sykdom som økte hos de overlevende etter atombombesprengningene i Hiroshima og Nagasaki. Etter oppdagelsen av røntgenstråler og radium ble man oppmerksom på farene. I 1928 ble ICRP (International Commission on Radiological Protection) opprettet. Uran finnes i naturen som 238U (99.28%), 235U (0.71%), og 234U (0.0058%). 235U kan spaltes og man må anrike denne ved en gassdiffusjonsprosess. I lettvannsreaktorer hvor vann brukes som moderator og til kjøling brukes 1-2 % av energien i uran. I formeringsreaktorer (breeder) hvor 238U og 232Th + neutroner gir 239Pu og 233U brukes 75 % av energien. Ved spalting av uran eller plutonium fås en rekke fisjonsprodukter (fisjon-lat. findere=spalte). Jo lenger tid uranstavene i en kjernereaktor bestråles med nøytroner, jo større mengde fisjonsprodukter bygger det seg opp. Etterhvert blir det så meget av slike produkter at de "forgifter" reaktoren ved å fange inn nøytroner som skulle ha vært brukt til å spalte uran. Uranstavene må da regenereres i en gjenvinningsanlegg for kjernekraftavfall.
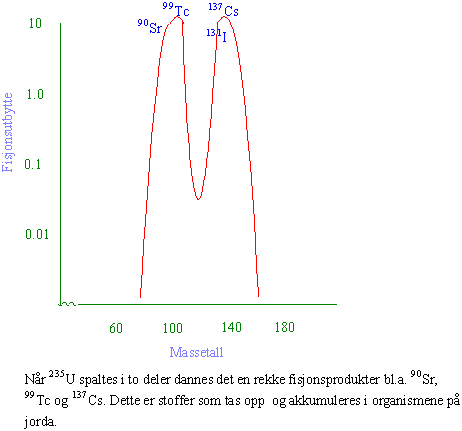
I august 1963 ble prøvestansavtalen undertegnet av U.S.A, U.S.S.R og Storbritannia. Frankrike og Kina forsatte imidlertid sine atombombeprøver i atmosfæren. Siden 1957 har det vært minst 16 større atomuhell (eks. Windscale-reaktoren 7.10.1957, Three Mile Island reaktoren U.S.A. 28.3.1979, Tsjernobylreaktoren Sovjetunionen 26.4.1986). Windscale skiftet navn til Sellafield. Det ble brukt panserbrytende granater med utarmet uran (DU-ammunisjon, "depledted uranium") i krigen mot Irak (1991), og i NATOs krigføring mot Jugoslavia (1999), en krig også Norge deltok i. De to atomreaktorene i Norge produserer også radioaktivt avfall. I Halden-reaktoren testes MOX-brensel ("mixed uranium-plutoniun dioxide") bl.a. produsert ved gjenvinningsanlegget i Sellafield, og som skal brukes i formeringsreaktorer.
Radioaktivt cesium følger med kalium inn i plantene
Opptaket av radioaktivt cesium i planter, 134Cs og 137Cs med halveringstider henholdsvis 2 og 30 år, har vært ansett som et av de største miljøproblemene ved radioaktiv forurensning. Resultatet etter Tsjernobylulykken i 1986 kommer vi til å merke i minst 50 år til hos oss. Cesium bindes sterkt i jorda og kan gradvis gjøres tilgjengelig for plantene. Kalium og cesium hører begge med til alkalimetallene i det periodiske system og har derved mange like kjemiske egenskaper. Innholdet av kalium er høyt i plantene og opptak og tilgang på kalium vil ha stor betydning for opptaket av radioaktivt cesium.
Jorda inneholder negativt ladete kolloider bestående av aluminiumsilikater (leirpartikler 1 -100 m) og humussubstanser. Ioner med positiv elektrisk ladning (kationer) bindes til kolloidene. Jo større ladning kationene har desto sterkere bindes de til kolloidene. For kationer med samme ladning bindes de med minst ioneradius i hydratisert tilstand hardest. Et ion (gr. ion= vandrer) er et atom med elektrisk ladning. m
Vi får følgende rekke av kationer hvor de lengst til venstre bindes hardest til kolloidene:
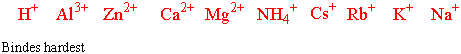
Vi ser at cesium bindes hardere til kolloidene enn kalium. Kalium kan bli byttet ut av alle ionene til venstre for seg i rekken over, inklusivt av cesium. Leirmineralene er det endelige forvitringsprodukt av silikatmineralene. De kan ha to sjikt (kaolinitt), tre (illitt, vermikulitt, montmorillonitt) eller flere sjikt (kloritt). Leirmineralene har store ytre og indre overflater og har stor evne til å binde vannmolekyler og ioner mellom sjiktene. I et land som Norge som utsettes for store mengder surt regn vil etterhvert cesium frigis fra de øverste par cm av jordlaget og vil kunne bli gjort tilgjengelig for plantene. Cesium havner også etterhvert ut i vann og vassdrag. Kalium bindes lite til organiske forbindelser i jorda, slik at de organiske kaliumreservene er små . Radioaktivt cesium i jord og vegetasjon i våre områder stammer fra kjernevåpenprøver og ulykker ved kjernekraftverk. Få måneder etter nedfall av radioaktivt cesium minsker betydningen av avsetningen på overflatene av vegetasjonen. Større betydning får da overføringen av radioaktive nuklider fra jord til planter og transport i næringskjedene. Fysiske, kjemiske og biologiske faktorer påvirker hvor fast de radioaktive nuklidene er bundet i jorda og hvor tilgjengelig de er for plantene.

I arktiske og alpine strøk er vekstsesongen kort, sommertemperaturen lav og nedbrytningsprosessene går sakte. Dette har stor betydning for den biologiske halveringstiden og langlevete fisjonsprodukter akkumuleres derfor i vegetasjonen i alpine strøk. Lav og sopp har stort opptak av cesium. Mykorrhiza vil derfor ha stor betyning for opptaket av radioaktive nuklider i vegetasjonen.
Radioaktivt strontium følger med kalsium
90Sr (strontium) har halveringstid ca. 28 år. Strontium hører med i gruppen jordalakaliemetallene i det periodiske system. Radioaktivt strontium (90Sr) vil følge kalsium inn i plantene. Fra plantene følger strontium næringskjeden videre. Hos mennesker og dyr vil strontium lagres i beinvevet. Planter som f.eks. blåbær kan ha et høyt innhold av ikkeradioaktivt strontium.
Radioaktivt technesium følger med mangan
Technesium (Tc) har bare ustabile radioaktive isotoper og hører hjemme i mangangruppen i det periodiske system og tas opp av plantene sannsynligvis sammen med mangan. Teknesium er et av spaltningsproduktene fra brenselsstaver i atomreaktorer og er et resultat av menneskelig aktivitet. Utslipp av teknesium fra gjenvinningsanlegget for brukt kjernebrensel i Sellafield i England er blitt funnet igjen i alger langs norskekysten. 99Tc har en halveringstid på ca. 213.000 år. Når det i leserinnlegg blir henvist til 99mTc brukt i nukleærmedisin har denne isotopen en halveringstid på bare 6.02 timer.
Deinococcus radiodurans er en ekstrem stråleresistent bakterie isolert nær atomreaktorer og andre strålekilder.
Presseklipp
Etter at bønder i Halden-området hadde spredd radioaktivitet utover jordene sine i 9 år kunne vi lese følgende i tidsskriftet Nature 26. april/ 410 (2001) 1016-1017 fra News in brief:
Waste mix-up creates radioactive fertilizer.
Farmers in nuclear-free Norway have been spreading low-level radioactive waste on their land for nine years after a pipeline mix-up, it was revealed last week. The country's Institute for Energy Technology (IFE) has admitted that, between 1991 and 1999, cooling water from a research reactor that should have been piped out to sea was instead directed into sewers beneath the city of Halden in southeast Norway. Some of the resulting sewage sludge containing the nuclear waste was sold to farmers for use as fertilizer. An IFE spokesperson insisted that there was no risk to health, as radioactive emissions from the waste water were well within safety limits. The pipeline has now been correctly connected.
Det var også en liten notis i Aftenposten morgen 18-04-2001: Atomavfall på avveie i Halden. Innleggene i Aftenposten var av følgende type Ny nordisk protest mot atomutslipp (21-08-2001). Sellafields stråler når Svalbard (19-08-2001). Professor går mot Børge Brendes Sellafield-utspill - Protesten ren populisme (19-12-2001). Leserbrevene i Aftenposten morgen har vært av følgende type: Nordisk Sellafield-motstand lite troverdig(09-10-2001). Forurensningen fra Sellafield ufarlig (18-10-2001). "Meningsløst og useriøst ?"(28-12-2001)
Langsiktige effekter
Plantene vil ta opp radioaktive isotoper og de vil å denne måten kunne akkumuleres i næringskjedene. Når slike radioaktive nuklider desintegrerer i nær kontakt med DNA i cellene vil enhver utsendelse av stråling gi mulighet til å få dannet en mutasjon i DNA. Hvilke langsiktige konsekvenser en slik økt mutasjonsfrekvens vil gi kjenner vi ikke rekkevidden av. Den kommer i tillegg til den naturlige bakgrunnsstrålingen. Saken gjelder ikke bare det rent strålingstekniske. Den har også en følelsesmessig og moralsk side. Med hvilken rett har vi lov til å bruke naturen som søppelfylling for antropogene langlevete radioaktive isotoper, DDT, PCB, dioksiner, tungmetaller, bromerte flammehemmere, organiske metallforbindelser etc., også med tanke på framtidige generasjoner ? Jeg er ikke sikker på at folk flest vil slå seg til ro med at litt radioaktivitet i maten er "helt ufarlig". På 1960-tallet var slagordet i kampen mot atomkraft og atombomber: Bedre aktiv i dag, enn radioaktiv i morgen. Den industrialiserte verdens levesett har tilpasset seg et energiforbruk som baserer seg på atomkraft og et enormt forbruk av olje og gass, med de problemene dette helt opplagt kommer til å skape på lang sikt. Inge Grødums tegning i Aftenposten 31-10-2001 er illustrerende: "Du ser litt tufs ut, Tellus. Hva er i veien ?" sier planeten Saturn. "Jeg har fått Homo sapiens" er svaret fra vår snufsete planet.