
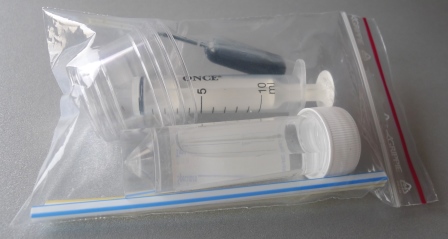
Utstyr til 2 elever
3 plastskåler
10 mL sprøyte
2 sugerør
BTB-løsning
helt rent vann
NB! Til dette forsøket kan vi ikke bruke springvann eller kjøpt mineralvann da det kan være bufret . (Vannet fra Oslo vannverk skal ha pH mellom 6,5 og 9,5. Middelverdien i 2012 var 7,65.)
Bakgrunn
Mengden karbondioksid (CO2) i luften øker langsomt pga forbrenning av kull, olje og naturgass (som alle inneholder karbonatomer (C)). Karbondioksid er en gass ved vanlig trykk og temperatur, og atmosfæren inneholder i dag 0,04 % dvs at fire av ti tusen molekyler i luften er karbondioksidmolekyler. Karbondioksid er nødvendig for alle grønne planter. Luft vi puster ut inneholder omtrent ti ganger så mye karbondioksid som det er i atmosfæren. I alt vann som er i kontakt med luft, er det noe oppløst karbondioksid og en del av den oppløste gassen har reagert med vannet. Hvis vi blåser ned i vannet med et rør, øker vi mengden karbondioksid som er løst i vannet. Mer karbondioksid reagerer med vannet og gir karbonsyre, så likevekten forskyves til høyre. Karbonsyre gjør at vannet blir surere. Etter hvert som eleven blåser mer luft ned i vannet, vil mer karbondioksid løses i vannet, og mengden karbonsyre i vannet øker, til vi når likevekt.
Indikatoren (BTB) er tilsatt vannet for å måle surheten i vannet. Når mengden karbonsyre i vannet endres ved tilsetting av karbondioksidgass, endres fargen på løsningen, se figuren.
For alle gasser gjelder at det løses mer gass i kaldt vann enn i varmt vann. Karbondioksidgassen i løsningen kan derfor fjernes enten ved vanlig koking eller ved «koking» ved lavt trykk ved hjelp av en sprøyte. Da forskyves likevekten til venstre fordi karbondioksidgassen drives ut av løsningen slik at konsentrasjonen av karbondioksid i løsningen blir mindre.
Fremgangsmåte og observasjoner
1. Tøm 3 mL vann i en plastskål (skål 1) og 6 mL i en annen (skål 2). Tilsett 2 dråper BTB til skål 1 og 4 dråper til skål 2. Tilsett litt mer BTB hvis fargen ikke er tydelig, dobbelt så mye i skål 2 som i skål 1.
2. Skål 1 skal du la stå som kontroll.
3. Blås med sugerøret ned i skål 2 til du får en tydelig fargeforandring.
4. Du skal fjerne oppløst gassen med «koking» ved lavt trykk ved hjelp av sprøyten.
a) Sug opp 3 mL av løsningen i skål 2.
b) Sett en finger foran åpningen og trekk stempelet ut så langt du kan uten å trekke det helt ut av sprøyten. Med fingeren foran åpningen og stempelet fremdeles uttrukket, rister du kraftig. Hold sprøyten med åpningen opp. Ta vekk fingeren fra åpningen så luft slipper inn. Skyv så all luft ut av sprøyten. Det er ikke nødvendig at vannet koker, men det er viktig å riste godt.
c) Gjenta b) minst ti ganger
5. Tøm innholdet i sprøyten i den tomme plastskålen (skål 3).
6. Beskriv fargene i de tre skålene og noter.
Resultater og spørsmål
a) Hvordan påvirkes likevekten: karbondioksid + vann ⇌ karbonsyre
av mengden karbondioksid i luften som vannet er i kontakt med og av temperaturen på vannet?
b) Hvordan påvirkes surhetsgraden i havene av mengden karbondioksid i atmosfæren?
c) Hvorfor blir påvirkningen forskjellig i forskjellige havområder?
Forslag til videre undersøkelser
Gjennomfør forsøket over med forskjellige typer vann for eksempel springvann eller kjøpt mineralvann, med og uten karbondioksid.
Risikovurdering
Egenskaper ved stoffene: Ingen merkepliktige stoffer eller løsninger.
Faremomenter ved gjennomføringen: Ingen
Spesielle tiltak: Ingen
Avfallshåndtering: Alle løsninger tømmes i vasken. Annet avfall sorteres og legges i rett avfallsbøtte eller kastes som restavfall.
Aktuelle læreplanmål
naturfag etter 7. årstrinn
- gjøre rede for bruken av noen energikilder før og nå, og innhente informasjon og statistikk fra ulike kilder for å beskrive og diskutere mulige konsekvenser av energibruken for miljøet lokalt og globalt
- beskrive sentrale egenskaper ved gasser, væsker, faste stoffer og faseoverganger ved hjelp av partikkelmodellen
- gjennomføre forsøk med ulike kjemiske reaksjoner og beskrive hva som kjennetegner dem
naturfag etter 10. årstrinn
- formulere testbare hypoteser, planlegge og gjennomføre undersøkelser av dem og diskutere observasjoner og resultater i en rapport
- undersøke og klassifisere rene stoffer og stoffblandinger etter løselighet i vann, brennbarhet og sure og basiske egenskaper
- forklare hvordan vi kan produsere elektrisk energi fra fornybare og ikke-fornybare energikilder, og diskutere hvilke miljøeffekter som følger med ulike måter å produsere energi på